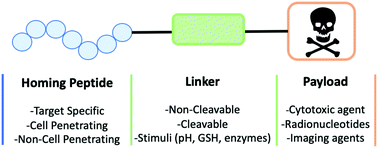
Antikor-İlaç Konjugatları (ADC'ler) tedavisinde devam eden ilerlemeye rağmen, bazı zorluklar devam etmektedir. Örneğin, ADC'lerin karmaşık yapısı yüksek üretim maliyetlerine ve uzun yarı ömre yol açar, bu da plazmada uzun süre maruz kalma nedeniyle sistemik toksisiteyi artırır. Sonuç olarak, Peptit-İlaç Konjugatları (PDC'ler) umut verici bir alternatif olarak ortaya çıkmıştır. PDC'ler üç bileşenden oluşur: bir hedef arama peptidi, bir bağlayıcı ve bir faydalı yük ilacı. Tümör yüzeyi reseptörlerine yönelik hedef peptitlerin yüksek afinitesinden yararlanan PDC'ler, faydalı ilacı doğrudan hedefe iletir.

PDC Yüklerinin Formları
PDC'ler çeşitli yük türlerini taşıyabilir. Bunlar paklitaksel veya gemsitabin gibi geleneksel kemoterapi ilaçları olabilir. Radyoaktif izotoplar aynı zamanda kesin hastalık teşhisi ve hedefe yönelik radyoterapi için de kullanılır. Tanısal izotoplar arasında Flor-18 (18F), Bakır-64 (64Cu), Galyum-68 (68Ga) ve İyot-123 (123I) bulunur. Hedefleyici peptidlerle konjuge edilen bu izotoplar, tümör hücresi reseptörlerine bağlanarak, izotoplar tarafından salınan pozitronların saptanması yoluyla kötü huylu dokuların kesin lokalizasyonuna olanak sağlar. Hedefleyici peptitler İndiyum-111 (111In), Yttrium-90 (90Y) ve Lutesyum-177 (177Lu) gibi radyoaktif izotoplara bağlandığında, PDC'ler hedeflenen radyoterapi ajanları olarak işlev görür. PDC'lerin diğer yükleri arasında proteinler, antikorlar, peptitler ve nükleik asitler bulunur.

PDC'lerin avantajları
PDC'ler ADC'lere benzerlikler sunar ancak bazı sınırlamalarının üstesinden gelir. ADC'lerle karşılaştırıldığında PDC'ler daha küçük moleküler ağırlığa, daha iyi doku penetrasyonuna ve daha düşük immünojeniteye sahiptir veya hiç yoktur. Ayrıca PDC'lerin sentezlenmesi, saflaştırılması ve tanımlanması daha kolaydır, bu da üretim maliyetlerinin düşmesine neden olur. Peptit seçimini hedeflemek için siklizasyon teknolojisi, faj görüntüleme teknolojisi ve mRNA görüntüleme teknolojisindeki ilerlemelerle birlikte PDC ilaçlarının gelişimi hızlanmıştır. PDC'ler, küçük molekül hedefli ilaçlar, antikor ilaçları ve ADC'lerin ardından yeni nesil hedefli ilaçlar olmaya hazırlanıyor.
PDC'lerin Farmakokinetik Özellikleri
EmilimPDC'ler, geleneksel küçük moleküllerle karşılaştırıldığında nispeten büyük bir moleküler ağırlığa ve zayıf geçirgenliğe sahiptir. Gastrointestinal sistemdeki peptitlerin kararsızlığı nedeniyle, piyasadaki ve klinik aşamalardaki mevcut PDC'ler, emilim sürecini atlayarak intravenöz olarak uygulanır. Ayrıca kan dolaşımına veya lenfatik sisteme girerek deri altından veya kas içinden de uygulanabilirler. PDC'lerin ilaç olarak önemli bir dezavantajı, peptitlerin proteazlar tarafından hızla parçalanması ve böbrekler tarafından kolayca temizlenmesi nedeniyle in vivo olarak kararsızlıkları ve kısa yarı ömürleridir. Bu, özellikle yeterli tümör dokusuna nüfuz etmek için genişletilmiş dolaşımın gerekli olduğu katı tümör tedavisinde problemlidir. Stabiliteyi arttırmak ve yarı ömrü uzatmak için peptitlerin değiştirilmesi çok önemli bir stratejidir.
DağıtımPDC peptidleri iki türe ayrılır: Hücre Hedefleyici Peptitler (CTP'ler) ve Hücreye Nüfuz Eden Peptitler (CPP'ler). CPP'lerin hücrelere yönelik düşük özgüllüğü nedeniyle, genellikle PDC'lerde hedef peptitler olarak kullanılmazlar. PDC'ler tümörleri iki şekilde hedefler: 1) PDC'ler, tümör hücresi yüzeylerinde aşırı eksprese edilen reseptörlere bağlanır, endositoz yoluyla hücrelere girer ve lizozomlarda toksinleri salar; 2) PDC'ler tümör ortamındaki toksinleri serbest bırakır ve bunlar daha sonra tümör hücrelerine girip onları öldürür.
MetabolizmaPDC'ler in vivo olarak üç ana yolla metabolize edilir:
- Hedef Aracılı İlaç İmhası (TMDD): TMDD spesifik bir eliminasyon yoludur. PDC'ler hedef hücreler üzerindeki reseptörlere bağlanır, içselleştirilir ve lizozomlarda amino asitlere ve peptitlere parçalanır. Bununla birlikte, hücre yüzeylerindeki hedeflerin sayısı genellikle sınırlıdır, bu da TMDD'yi doyurulabilir hale getirir ve doğrusal olmayan farmakokinetik ile sonuçlanır.
- Spesifik Olmayan Metabolizma: Proteoliz ve spesifik olmayan pinositoz gibi hedef aracılı olmayan süreçler, küçük moleküllü sitotoksinlerin istenmeyen bölgelerde salınmasına neden olarak hedef dışı yan etkilere neden olabilir.
- İmmünojenisite: PDC'ler, ilacı nötralize eden ve bağışıklık sistemi tarafından temizlenen kompleksler oluşturan Anti-İlaç Antikorlarının (ADA'lar) üretimini uyararak immünojenisiteyi tetikleyebilir. Klinik öncesi hayvanlarda gözlemlenen immünojenite veya ADA yanıtlarının insan ADA yanıtlarını öngörmediğini belirtmek önemlidir.
BoşaltımMolekül ağırlığı renal filtrasyon eşiğinden (60 kDa) çok daha küçük olan PDC'ler böbrekler tarafından hızla temizlenerek tümörlerde sitotoksinlerin etkili bir şekilde birikmesi önlenir. Bu nedenle stabiliteyi arttırmak ve yarı ömrü uzatmak için PDC'lerin hedef peptitlerinde modifikasyonlar veya kimyasal değişiklikler gereklidir. Bazı peptitler veya PDC ilaçları için böbreklerden atılım birincil temizlenme yolu olabilir. Bu gibi durumlarda, IV uygulama sonrası bölmeli olmayan analizden (NCA) hesaplanan temizlenme oranının, hepatik kan akışından ziyade ilacın glomerüler filtrasyon hızına referans verilmesi gerektiğinin dikkate alınması çok önemlidir.
PDC'ler için Farmakokinetik Çalışma Stratejileri
PDC'ler doğası gereği, hem büyük hem de küçük moleküllü ilaçların özelliklerini birleştirerek ilaç dağıtımı için hedefleme stratejilerini kullanır. Göreceli istikrarsızlıkları ve hedefleme sorunları nedeniyle, faydalı yükün potansiyel zehirliliği özel dikkat gerektirir. İlaç tarama aşamasında, DMPK çalışmaları tam kan, plazma ve böbrek homojenatındaki peptitlerin ve PDC'lerin stabilitesini iyileştirmeye odaklanırken stabiliteyi ve yarı ömrü artırmak için in vitro ve in vivo metabolit tanımlama yoluyla PDC yapısını optimize etmeye devam eder. Yükün farklı organlara yönelik potansiyel toksisitesini değerlendirmek için projenin başlarında kemirgenlerde doku dağılım çalışmalarının yapılması tavsiye edilir.
Klinik aday aşamasında, yükün in vivo salınımını değerlendirmek ve doğrulamak için uygun in vitro modeller tanımlanmalıdır. İn vivo deneyler aynı anda PDC'nin kan konsantrasyonunu ve yükü ölçmelidir. Tekrarlanan doz koşullarında ADA etkilerinin izlenmesi tavsiye edilir. PDC'lerin hedefleme yeteneğini değerlendirmek için PD türlerinde doku dağıtım deneyleri yapmak gereklidir.
Sonuç ve Görünüm
ADC ilacı geliştirmedeki kapsamlı deneyime rağmen, PDC ilaçlarının geliştirilmesi basit bir yol değil, hem fırsatlar hem de zorluklarla dolu bir yoldur. ADC'lerle karşılaştırıldığında, peptitlerin doku özgüllüğü ve tümör hedeflemesi biraz daha düşüktür ve hedefleyici peptitlerin seçiminde önemli zorluklar ortaya çıkarmaktadır. Ek olarak, peptidlerin zayıf stabilitesi nedeniyle oral uygulama önemli ölçüde zorluk teşkil etmektedir. PDC'ler aynı zamanda analitik zorluklarla ve potansiyel hedef dışı etkilerle de karşı karşıyadır.
PDC ilaçlarının tasarımı, peptidleri ve çeşitli ilaç türlerini hedeflemenin avantajlarını birleştirir. Radyonüklid terapötik ilaçlar ve teşhis ajanlarına ilişkin son düzenleyici onaylar, bu ilaçların potansiyelini vurgulamaktadır. Devam eden klinik boru hatlarından elde edilen klinik sonuçların teşvik edilmesi, vaatlerinin altını daha da çiziyor. Çeşitli moleküler varlıkların konjugasyonu ve hedefleyici peptitler ile PDC ilaçlarının geliştirilmesi, gelecek için büyük bir potansiyele sahiptir.